来源:未知 时间:2025/02/18 作者:admin2021
这篇AnalyticalChemistry文章发表于2024年12月;文章的第一作者为Junyang Chen,通讯作者为Wei Li,工作单位为郑州大学基础医学院。该研究通过针对FAP蛋白糖基化的适配体筛选策略,成功开发出一种基于双适配体的表面增强拉曼散射(SERS)免疫夹心测定法,实现了对FAP的高灵敏度和高选择性检测,为癌症诊断提供了一种新的、高效且具有临床应用潜力的检测方法。


1.糖基化靶向适配体的筛选策略:研究者提出了一种针对FAP蛋白糖基化结构的适配体筛选策略,通过交替引入糖蛋白FAP和去糖基化FAP进行筛选,成功获得了针对FAP糖基化结构的高性能适配体。这种策略不仅提高了适配体的选择性,还为抗糖基化适配体的筛选提供了新的方法。
2.双适配体基底等离子体免疫夹心测定法(odA-PISA):研究者结合糖基化靶向适配体和蛋白结合适配体,构建了一种新型的双适配体基底等离子体免疫夹心测定法。该方法利用表面增强拉曼散射(SERS)技术实现了对FAP的高灵敏度和高选择性检测,检测限低至100 pg/mL,交叉反应性小于8%,显著优于传统方法。
3.适配体的结构优化与性能提升:通过截短策略对筛选出的适配体进行优化,去除了不必要的核苷酸,降低了成本并提高了结合性能。优化后的适配体(如Seq2T)展现出更低的表观解离常数(KD值低至9.74 nM)和良好的特异性,为实际应用提供了更高效的选择。
4.G-四链体结构的应用:研究发现筛选出的适配体具有形成G-四链体的潜力,并通过实验确认了其G-四链体结构。这种结构的发现不仅为适配体的稳定性提供了支持,还为设计具有更高亲和力和特异性的适配体提供了新的思路。
5.临床应用潜力:该研究不仅在实验室环境中验证了新方法的性能,还成功将其应用于癌症患者血清样本中FAP的检测,显示出良好的临床应用前景。与传统酶联免疫吸附测定(ELISA)相比,该方法具有更快的响应速度、更宽的检测范围和更低的成本,为癌症诊断提供了一种新的高效工具。
总体而言,这篇论文通过创新的适配体筛选策略和检测技术的开发,为FAP的检测提供了一种高灵敏度、高选择性的新方法,并为糖基化蛋白的适配体研究和临床应用开辟了新的方向。

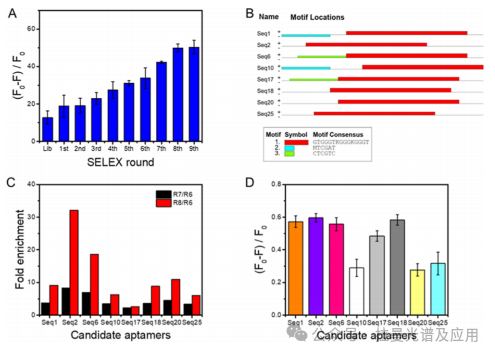 图(1)展示了适配体筛选过程中,特定单链DNA(ssDNA)的富集情况以及候选适配体的结合亲和力,表明随着筛选轮数的增加,ssDNA对目标FAP的结合能力逐渐增强,且在第八轮达到饱和,成功筛选出具有高亲和力的适配体候选序列。
图(1)展示了适配体筛选过程中,特定单链DNA(ssDNA)的富集情况以及候选适配体的结合亲和力,表明随着筛选轮数的增加,ssDNA对目标FAP的结合能力逐渐增强,且在第八轮达到饱和,成功筛选出具有高亲和力的适配体候选序列。
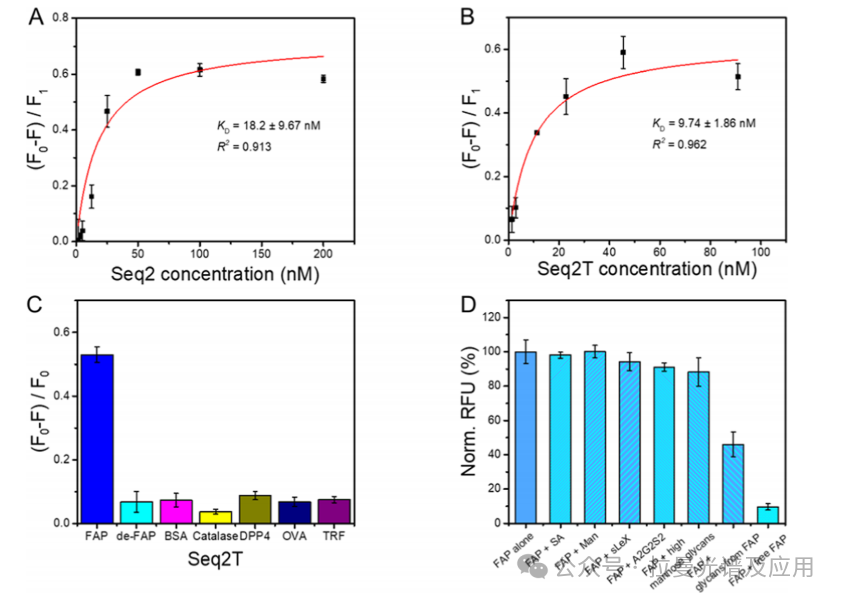
图(2)通过荧光法和生物层干涉(BLI)法评估了优化后的适配体(Seq2T)与FAP蛋白的结合亲和力,并测试了其特异性,结果表明Seq2T对FAP具有高亲和力(KD值低)且与其他蛋白质的交叉反应性极低,显示出良好的特异性。

图(3)展示了适配体Seq2T的二级结构预测以及与FAP蛋白的分子对接模型,揭示了Seq2T可能通过其G-四链体结构与FAP蛋白的糖基化位点附近的残基相互作用,从而实现对FAP的特异性识别。。
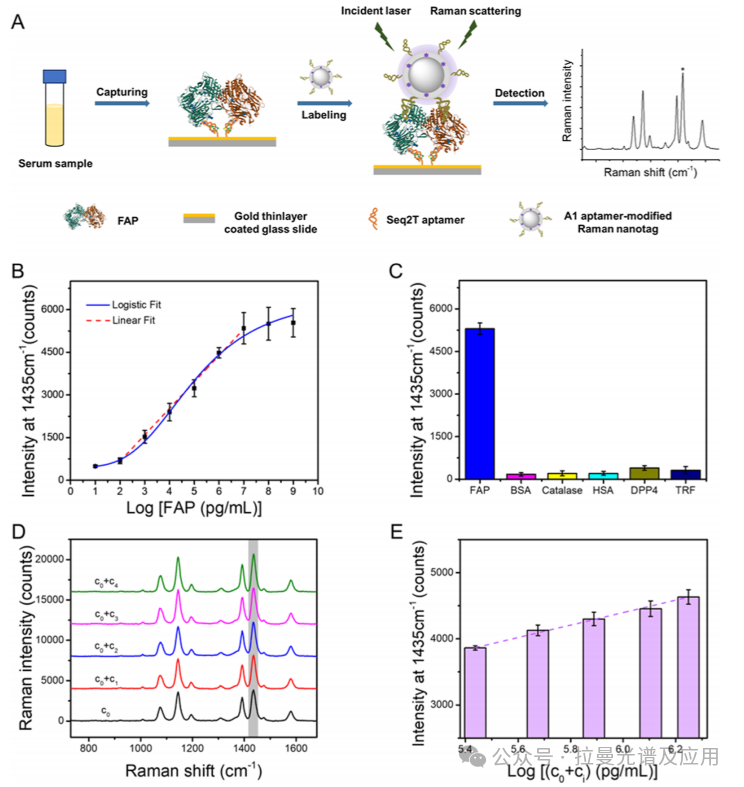
图(4)介绍了基于双适配体的表面增强拉曼散射(SERS)免疫夹心测定法(odA-PISA)的原理及其对FAP的检测性能,包括线性范围、检测限和选择性测试,结果表明该方法具有高灵敏度、高选择性,并成功应用于血清样本中FAP的定量检测。
· 点“阅读原文”下载全文

数据处理:定量分析与方法验证
模拟与计算:分子对接分析



