来源:未知 时间:2025/02/18 作者:admin2021
这篇Analytical Chemistry文章发表于2024年12月;文章的第一作者为Junyang Chen,通讯作者为Wei Li,工作单位为郑州大学基础医学院。该研究通过针对FAP蛋白糖基化的适配体筛选策略,成功开发出一种基于双适配体的表面增强拉曼散射(SERS)免疫夹心测定法,实现了对FAP的高灵敏度和高选择性检测,为癌症诊断提供了一种新的、高效且具有临床应用潜力的检测方法。

这篇论文的数据处理主要集中在通过表面增强拉曼散射(SERS)信号的定量分析来验证所开发的双适配体基底等离子体免疫夹心测定法(odA-PISA)的性能。研究者通过绘制校准曲线、计算检测限和定量限,以及对比不同样本的检测结果,全面评估了该方法的灵敏度、选择性和准确性。
线性关系:通过将不同浓度的FAP标准溶液添加到适配体修饰的阵列上,测量其对应的Raman信号强度,研究者建立了Raman强度与FAP浓度对数之间的线性关系。这一线性关系用于定量分析未知样本中的FAP浓度。
检测限(LOD):定义为信噪比(S/N)为3时对应的浓度,计算得到的检测限为10 pg/mL。
定量限(LOQ):定义为信噪比(S/N)为10时对应的浓度,计算得到的定量限为100pg/mL。这表明odA-PISA方法具有极高的灵敏度,能够检测到极低浓度的FAP。
交叉反应性:通过测试odA-PISA对FAP和其他五种干扰蛋白(包括人血清白蛋白)的Raman信号强度,评估该方法的选择性。结果显示,FAP的Raman信号远高于其他干扰蛋白,交叉反应性仅为3.3%至7.4%,表明该方法具有极高的选择性。
标准添加法:为了验证检测结果的准确性,研究者采用标准添加法,在血清样本中加入已知浓度的FAP标准溶液,然后通过odA-PISA方法进行检测。通过比较添加前后Raman信号的变化,验证了该方法在复杂生物样本中的适用性。
与ELISA对比:研究者还通过商业ELISA试剂盒对同一血清样本进行检测,对比两种方法的检测结果。结果显示,两种方法的检测结果一致,进一步验证了odA-PISA方法的可靠性和准确性。

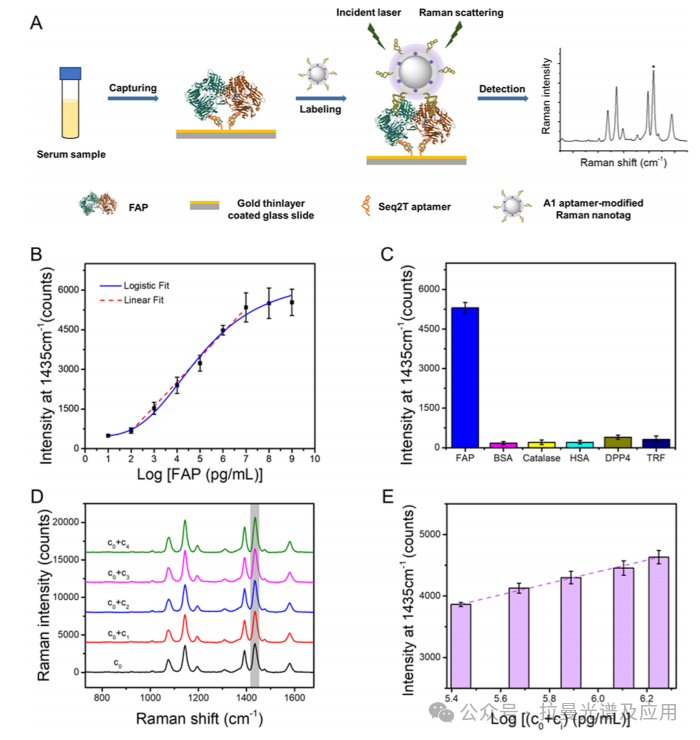 图4(B):展示了odA-PISA的Raman强度与FAP浓度对数之间的线性关系。图中绘制了不同浓度FAP标准溶液的Raman强度,拟合得到的线性方程:y=−1197.20+930.67x,相关系数 R2=0.997。该图表明odA-PISA在100 pg/mL至10 μg/mL的浓度范围内具有良好的线性响应,检测限为100 pg/mL。这表明该方法具有高灵敏度,能够检测到极低浓度的FAP。
图4(B):展示了odA-PISA的Raman强度与FAP浓度对数之间的线性关系。图中绘制了不同浓度FAP标准溶液的Raman强度,拟合得到的线性方程:y=−1197.20+930.67x,相关系数 R2=0.997。该图表明odA-PISA在100 pg/mL至10 μg/mL的浓度范围内具有良好的线性响应,检测限为100 pg/mL。这表明该方法具有高灵敏度,能够检测到极低浓度的FAP。
图4(D):展示了胆囊癌患者血清样本中加入已知浓度FAP标准溶液后的Raman光谱图。图中显示了不同浓度(c1至c4分别为200、500、1000和1500 ng/mL)的FAP标准溶液在血清样本中的Raman信号。通过标准添加法,研究者能够观察到随着FAP浓度的增加,Raman信号强度显著增强,这表明odA-PISA方法能够准确检测血清样本中的FAP。该实验验证了该方法在复杂生物样本中的适用性和准确性。
图4(E):展示了胆囊癌患者血清样本中FAP浓度的线性关系图。图中绘制了Raman强度与总FAP浓度(血清中初始浓度c0加上添加的浓度ci)的对数之间的线性关系。通过线性拟合,研究者发现Raman信号与FAP浓度之间存在良好的线性关系(y = −1250.96 + 941.16x,R² = 0.995),这进一步验证了odA-PISA方法在定量检测血清样本中FAP的可靠性。该实验结果表明,该方法可以用于实际临床样本的检测。
通过系统的数据处理,研究者不仅验证了odA-PISA方法的高灵敏度和高选择性,还通过与传统ELISA方法的对比,进一步证明了该方法的准确性和可靠性。



